ЛАУРЕАТ В НОМИНАЦИИ «DISCOVERY/ОТКРЫТИЕ»
ЗА ИЗОБРЕТЕНИЕ РЕАКЦИИ, ОПРЕДЕЛИВШЕЙ КЛИК-ХИМИЮ И ПРЕОБРАЗИВШЕЙ МОЛЕКУЛЯРНЫЕ НАУКИ И ХИМИЮ ЖИВЫХ СИСТЕМ

ВАЛЕРИЙ ФОКИН
PhD по химии, профессор Университета Южной Калифорнии (США)
Более 59 000 цитирований, более 300 публикаций, h-index = 83
О лауреате
Достижение лауреата относится к области на стыке биологии, химии и медицины. Валерий Фокин изобрёл реакцию, которая позволила перевернуть концепцию клик-химии и с новым качеством заглянуть в мир живого, создать новые диагностические лекарственные средства.
В химии чаще всего реакция между веществами идёт не до конца: она может идти слишком медленно, могут иметь место какие-то побочные реакции. Поэтому длительное время химики мечтали об универсальных реакциях, идущих между большим количеством соединений, с высокой эффективностью и малым количеством побочных продуктов. Это позволила сделать клик-химия (от click – «щелчок», звукоподражание моменту, когда какая-то деталь вставляется на свое место и защелкивается).
В 2022 году за развитие клик-химии и биоортогональной химии Барри Шарплессу, Мортену Мельдалю и Каролин Бертоцци была вручена Нобелевская премия. Однако главную реакцию клик-химии, переопределивший сам термин открыл самостоятельно в 2002 бывший сотрудник Барри Шарплесса Валерий Фокин, который изобрел реакцию азид-алкинового присоединения, катализируемого медью в присутствии аскорбиновой кислоты (СuACC). Барри Шарплесс – автор первоначальной концепции клик-химии – неоднократно подчеркивал приоритет Фокина в создании метода СuACC.
Сейчас универсального набора реакций сборки любых сложных органических соединений до сих пор не существует, но клик-химия с использованием CuACC – это универсальная химическая «защелка», позволяющая «скреплять» между собой сложные фрагменты молекул.
На основе работ Валерия Фокина созданы системы визуализации ДНК, методы диагностики метастазов онкологических заболеваний, уже одобренный для клинического применения препарат для лечения метастатического рака молочной железы. В мире ежедневно проводятся многие тысячи реакций СuAAC для самых разнообразных клинических и научных целей, в первую очередь – для секвенирования последовательности генов. Это позволяет считать Валерия Фокина автором одной из важнейших технологий будущего, которая уже начинает приносить пользу человечеству в настоящем.
Валерий Фокин родился в 1971 году. В 1993 году он окончил химический факультет Нижегородского государственного университета имени Н.И. Лобачевского, а также получил степень бакалавра в Колледже Кальвина (сейчас – Университет Кальвина, Мичиган, США), куда поехал учиться на пятом курсе по программе обмена. В 1998 году в Университете Южной Калифорнии получил степень PhD, после чего остался в США. В настоящее время он является профессором Университета Южной Калифорнии (США).
-
Что такое «клик-химия»?
Концепция клик-химии сформулирована дважды нобелевским лауреатом по химии Барри Шарплессом. Он предполагал, что можно подобрать набор простых, надежных и быстро протекающих с высоким выходом реакций, при помощи которых можно легко и дешево синтезировать самые разнообразные сложные органические молекулы (изначально Шарплесс размышлял о синтезе молекул-кандидатов в лекарственные препараты). Слово «клик» в данном случае – звукоподражание щелчку застежки-фастекс, которая закрывается «до щелчка». Однако изобретение лауреата и его дальнейшее применение определило клик-химию несколько иначе.
За что Валерий Фокин удостоен премии «ВЫЗОВ»?
Премия «ВЫЗОВ» в номинации «Открытие» в 2025 году присуждена Валерию Фокину (Университет Южной Калифорнии, США) за изобретение реакции, определившей клик-химию и преобразившей молекулярные науки и химию живых систем.
Главное достижение лауреата – это изобретение реакции азид-алкинового присоединения (азиды – молекулы, содержащие группу N3, алкины – углеводороды, содержащие тройную связь углерод-углерод). Точнее – изобретение той ее формы, которая катализируется получаемыми в самой реакционной смеси ионами меди (I). А получаются эти ионы добавлением в реакцию медного купороса и аскорбиновой кислоты, которая восстанавливает двухвалентную медь в одновалентную.
Сама реакция азид-алкинового присоединения была открыта в позапрошлом веке, в 1893 году американским химиком Артуром Михаэлем. Это реакция присоединения между азидами и алкинами с образованием 1,2,3-триазолов. В 1960-году Рольф Хьюсген детально исследовал азид-алкиновое присоединение, за что реакция получила его имя.
Азид-алкиновое циклоприсоединение по Хьюсгену – требует нагрева и длительного времени
Однако эта реакция требовала нагрева, шла достаточно капризно и долго: первооткрывателям для синтеза требовалась температура около 100 градусов Цельсия и почти сутки нагрева (18 часов).
И только самостоятельное изобретение Фокина принципиально изменило ситуацию. Его реакция идет в растворе, всегда и везде – в том числе в живой клетке. При этом органических азиды «биоортогональны» (термин Каролин Бертоцци) – их нет в живой клетке, и, будучи добавленной к биомолекулам, азидная группа инертна и не реагирует ни с чем, пока к ним не добавлены алкин и медь. А к алкину может быть прикреплено что угодно: флуоресцентный маркер, химиотерапевтический агент и так далее.
Созданная Валерием Фокиным реакция изменила предназначение клик-химии. Вместо конструктора, в котором клик-реакции собирают сложные молекулы из простых частей, вставляя их «до щелчка», науки (не только химия, но и медицина, биология, фармакология и генетика) получили универсальную и надёжную молекулярную «застёжку», которой можно «пристегивать» фрагменты молекул к другим биомолекулам или частям живой клетки – хоть к молекуле ДНК, хоть к антителу.
Лауреат особенно отмечает, что его работа – это именно изобретение, а не открытие или исследование. По мнению Валерия Фокина, открыть можно только то, что существует в природе (и можно сделать это случайно – как, например, это сделал, Александр Флеминг, забыв помыть чашки Петри перед отпуском и открыв пенициллин). Изобрести можно только что-то полностью новое. Исследование же это – «гонка за знаниями», которая может привести к открытию или изобретению. А может и не привести.
Где применяется CuAAC?
Через два десятка лет после создания CuAАC нашла широкое применение во многих областях науки. Это синтезы триазолов (из более чем 27 тысяч синтезов, опубликованных к 2025 году, 25 тысяч – при помощи CuAAC), это визуализация многих процессов в клетке: введенные в организм аминокислоты или азотистого основания с азидными радикалами позволяют при помощи флуоресцентных маркеров с алкиновыми «хвостиками» напрямую визуализировать синтез белка в клетке или синтез ДНК.
Метод CuAАC используется для «пришивания» терапевтических агентов к антителам, доставляющим их в патологический очаг. Один из самых успешных примеров, дошедших до клинической практики - препарат «Троделви» (фармакологическое наименование – сацитузумаб говитекан), коньюгат моноклонального антитела для лечения трижды негативного рака молочной железы.
Еще одно важное применение CuAАC, используемое ежедневно – это секвенирование (установление порядков нуклеотидов) ДНК. Один из новых методов секвенирования использует клик-реакцию для «прочтения» генетического кода. Речь идет о методе ClickSeq, который коммерциализован и используется в стандартных секвенаторах.
-
Научный комитет Национальной премии в области будущих технологий «ВЫЗОВ» присудил премию 2025 года в номинации «Открытие» за изобретение реакции, определившей клик-химию и преобразившей молекулярные науки и химию живых систем профессору Валерию Фокину (Университет Южной Калифорнии, США).
Химический контекст
В химии большинство реакций несовершенно: они идут медленно, дают побочные продукты или работают только в узких условиях. Поэтому исследователи давно мечтали о «универсальных» реакциях — быстрых, селективных, чистых и применимых к широкому спектру молекул. Среди исторических примеров — реакция Дильса–Альдера (Нобелевская премия 1950 года). В 2001 году лауреат Нобелевской премии Барри Шарплесс сформулировал концепцию клик-химии — сборки сложных молекул из небольших фрагментов с помощью высокоэффективных реакций, «щелкающих» как конструктор.
Создание CuAAC
В том же году Валерий Фокин, тогда уже молодой профессор Института Скриппса, независимо разработал реакцию, ставшую сердцем клик-химии. 30 октября 2001 года в его лабораторном журнале появилась запись о реакции азидов с алкинами в присутствии ионов одновалентной меди — медь-катализируемом азид-алкиновом циклоприсоединении (CuAAC). Сам лауреат подчёркивает, что CuAAC — именно изобретение, а не открытие: эта реакция не существует в природе и была сознательно сконструирована как новый химический инструмент. Несмотря на то, что приоритет Валерия Фокина в создании CuAAC никогда не оспаривался (включая многочисленные публичные выступления Шарплесса), Нобелевская премия 2022 года за развитие клик-химии была вручена Барри Шарплессу, Мортену Мельдалю и Каролин Бертоцци.
Как CuAAC изменила концепцию клик-химии
Работа Фокина не только создала основную реакцию клик-химии, но и расширила её смысл. То, что все компоненты CuAAC, алкин, азид и Cu(I), отсутствуют в живых организмах, позволило использовать эту реакцию как биоортогональный «молекулярный замок», к которому можно «пришивать» биомолекулы:
• антитела
• флуоресцентные метки
• терапевтические молекулы
• носители лекарств
CuAAC стала надёжным способом молекулярной сборки прямо в живых клетках и тканях.
Практическое значение
Работы Валерия Фокина привели к появлению технологий, широко используемых в науке и медицине, включая:
• системы визуализации Thermo Fisher Click-iT™
• методы секвенирования Illumina
• одобренный FDA препарат Trodelvy® для лечения метастатического рака молочной железы
Ежедневно по всему миру проводится множество тысяч реакций CuAAC — в химии, биологии, биомедицине, материаловедении и диагностике. Это позволяет считать Валерия Фокина как автора одной из ключевых технологий XXI века, уже приносящей реальную пользу человечеству.
-
Клик-химия, CuACС- реакция, ее переопределившая и современные приложения CuACC
Что такое клик-химия?
Саму идею клик-химии выдвинул профессор Института Скриппс Барри Шарплесс, сейчас – один из двух в истории дважды нобелевский лауреатов по химии.
Комбинаторная химия в 1990-е годы вызывала большой интерес, особенно для разработки лекарств. Были синтезированы большие коллекции соединений, также известные как «комбинаторные библиотеки», которые затем тестировались на биоактивность.
Шарплесс подумал, что эффективное производство таких коллекций соединений значительно выиграет от более «упрощенного» процесса синтеза, когда каждое соединение может быть получено с использованием ограниченного набора надежных и эффективных реакций.
Вместо того, чтобы полагаться на множество возможных методов, каждый - со своими специфическими областями применения и ограничениями, он предположил, что многие востребованные в фармакологии структуры можно будет «собирать» с помощью более общих, надежных и – что важно – высоковыходных реакций.
В 2001 году, когда Шарплесс получил свою первую Нобелевскую премию за хиральный катализ, у него вышла статья Click Chemistry: Diverse Chemical Function from a Few Good Reactions, которую Шарплесс выпустил с соавторами – Хармутом Кольбом и М.Г. Финном (он даже в аннотации авторов М.Г., без расшифровки), в которой и формулировалась такая концепция клик-химии.
Однако изобретение «главной» клик-реакции бывшим сотрудником Шарплесса Валерием Фокиным и ее дальнейшее развитие де-факто переписало концепцию клик-химии в ее реальном применении.
Почему «клик»?
В формулировке Шарплесса клик-химия представляла собой набор реакций, которыми надежно, как в конструкторе с «защелками», из небольшого набора реакций вы можете собирать любые сложные молекулы. Некоторые такие реакции были известны очень давно: например, реакция Дильса-Альдера, циклоприсоединение 1,3-диенов к двойной связи идет почти всегда, надежно и позволяет «собирать» различные шестичленные циклы. Авторы реакции, Отто Дильс и Курт Альдер, в 1950 году были удостоены Нобелевской премии по химии.
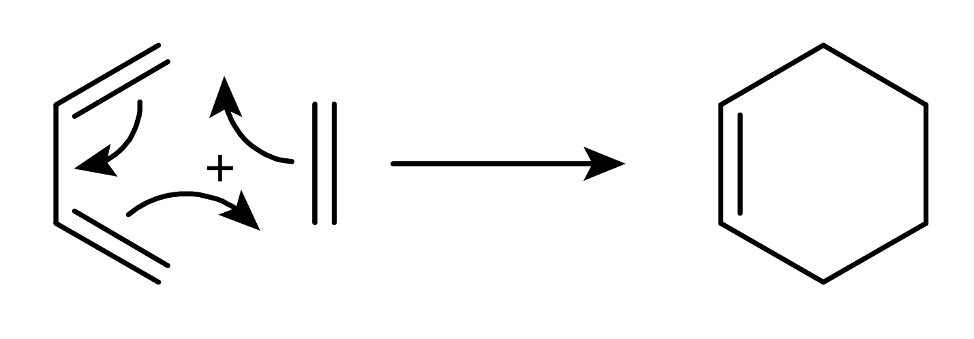
Реакция Дильса-Альдера
Идеологически «Дильс-Альдер» очень близок к первоначальной концепции клик-химии, которая, однако, не сработала. До сих пор, через четверть века после формулировки Шарплеса-Кольба-Финна, не существует некоего универсального набора реакций, который бы позволял быстро «собирать» молекулы, равно как и не существует универсального метода функционализации сложных молекул (способа, позволяющего заменить в произвольном месте сложной органической молекуле, например, группу -OH на -СH3, а -CH3 на -С2H5 или -Cl).
Однако изобретение Валерия Фокина (о котором чуть позже), с одной стороны, спасло саму концепцию, а с другой стороны, переопределило её.
Лучше всего понимание того, почему клик-химия названа так, дает сам лауреат в интервью журналу «Химия и жизнь»:
«Представьте себе популярную застежку фастекс, которую используют на рюкзаках. Она будет застегиваться всегда: в тепле, на снегу, на суше, под водой. И скреплять будет что угодно: клапан рюкзака, ремень сумки, брелок на телефоне. Собственно, слово «клик» появилось в названии именно по аналогии со звуком защелки, — говорит Валерий Фокин. — Теперь уменьшим нашу застежку до размеров молекулы. Защелка и пряжка будут химическими соединениями, как, например, азид и алкин. Они друг друга не замечают, пока не добавлена медь. И вот тогда они моментально защелкиваются, образуя замок из пяти атомов».
То есть в лице клик-химии вместо метода-конструктора, позволяющего собрать любую молекулу, химия, медицина и науки о жизни получили надежную молекулярную застежку, которая позволяет соединять совершенно разные фрагменты молекул. Что же это за застежка? Ей оказалась реакция, открытая еще в XIX веке, но изобретенная заново Валерием Фокиным (лауреат настаивает, что это было именно изобретение, а не открытие).
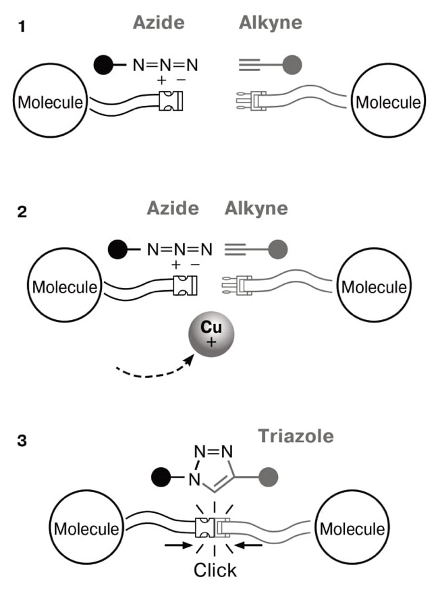
Клик-химия как застежка
Главная реакция клик-химии, или что сделал лауреат?
Сама реакция, о которой пойдет речь как оказалось, была открыта ещё в 1893 году американским химиком Артуром Михаэлем. Это – реакция присоединения между азидами и алкинами с образованием 1,2,3-триазолов. В 1960-году Рольф Хьюсген детально исследовал азид-алкиновое присоединение, за что реакция получила его имя.
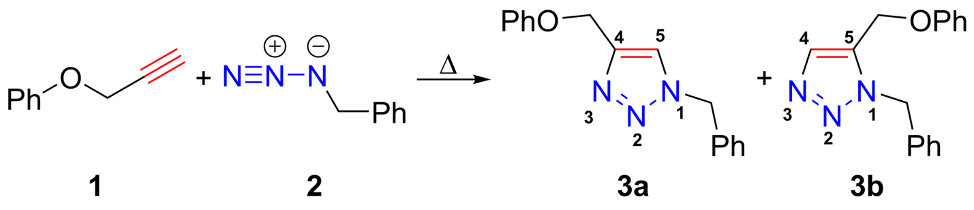
Азид-алкиновое циклоприсоединение по Хьюсгену – требует продолжительного времени и повышенной температуры
Однако эта реакция требовала нагревания, шла достаточно капризно и долго: у её первооткрывателей для синтеза требовалась температура около 100 градусов Цельсия и почти сутки нагрева (18 часов).
В 2002 году с разницей в несколько недель вышло две независимые статьи: Мортена Мёльдаля и Валерия Фокина, которые показали, что азид-алкиновое циклоприсоединение может катализироваться одновалентной медью. Однако Мёльдаль работал напрямую с медью (I), а реакцию проводил в смолах – в твердой фазе. Работа Фокина была совсем иной. Гениальная догадка – реакцию можно проводить, получая Cu (I) in situ. Достаточно взять немного медного купороса и… обыкновенную аскорбинку. Да, для реакции Фокин просто взял порошок аскорбиновой кислоты, который пил сам.
Оказалось, что катализируемое медью азид-алкиновое циклоприсоединение (CuAAC) полностью удовлетворяет всем условиям «реакция для клик-химии». Идет всегда и везде, с почти идеальным выходом, и только в присутствии двух этих компонентов – ионы меди (II) и аскорбиновая кислота. В руках химиков, медиков, фармакологов, генетиков и биологов оказался инструмент, который позволял не только получать триазолы, но и «сшивать» фрагменты различных биомолекул. Однако Нобелевскую премию 2022 года получили Барри Шарплесс (соавтор Фокина по статье, но всегда подчеркивавший, что CuAAC – «на 100% - творение Фокина единолично»), Мортен Мёльдаль и Каролин Бертоцци, создавшая вариант азид-алкинового циклоприсоединения, катализируемого напряжением – для этого нужен напряженный циклоалкин, например, циклооктин. Каролин стала первым ученым, указавшим на особую интертность, «биоортогональность» органических азидов.
Тем не менее, практика и время показали, что из всех «клик-реакций» действительно «кликабельной» оказалась CuAAC Валерия Фокина.
Практические приложения CuACC
В органической химии CuACC стала самой главной реакцией синтеза триазолов: с 2001 по 2025 год в химической литературе описано более 27 тысяч синтезов с образованием триазольного цикла, из которых 25 тысяч было синтезировано при помощи реакции азид-алкинового присоединения, катализируемого медью в присутствии аскорбиновой кислоты.
Способность CuACC «пришивать» функциональные фрагменты молекул – терапевтические агенты, флуоресцентные маркеры и так далее – к нужным участкам живой клетки начала активно использоваться в науках о жизни. Например, в 2008 году метод был использован для визуализации процесса синтеза ДНК – без использования радиоактивных меток или антител и без денатурации ДНК, а в 2010 году СuACC использовался для того, чтобы in situ визуализировать синтез белка в живых нейронах.
Одно из важных практических применений CuACC, спасающее тысячи жизней ежегодно – препарат «Троделви» (фармакологическое наименование – сацитузумаб говитекан), коньюгат моноклонального антитела для лечения трижды негативного рака молочной железы.
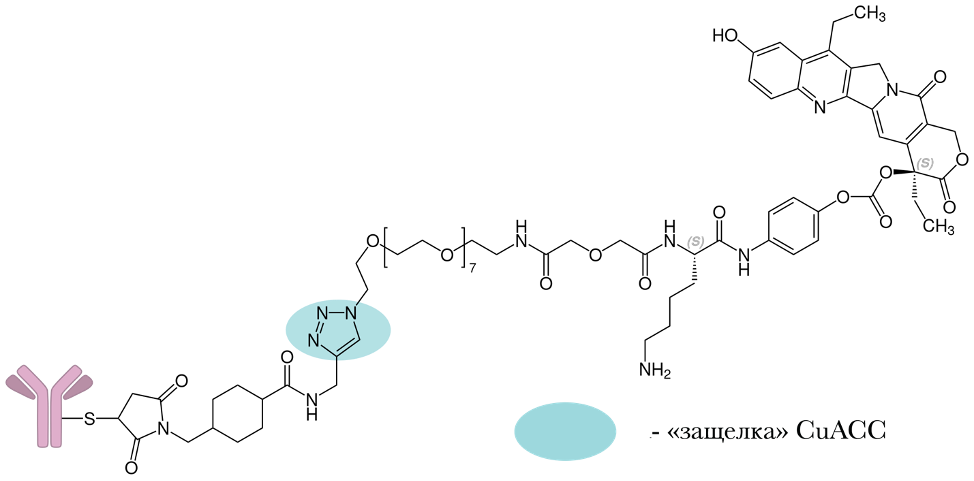
Схема «привеска» к антителу в молекуле препарата Троделви. Автор: Алексей Паевский, Syed, Y.Y. Sacituzumab Govitecan: First Approval. Drugs 80, 1019–1025 (2020).
Этот сложный препарат состоит из антитела, которое избирательно связывается с кальциевым каналом, в огромных количествах появляющегося именно в опухолевых клетках. На это антитело «навешены» целых семь активных метаболитов химиотерапевтического препарата иринотекана, которые действуют в тысячу раз сильнее самого препарата. Антитело «привозит» эти молекулы строго в клетки опухоли и «сбрасывает» их при помощи гидролиза мостиков, которым химиотерапевтические агенты привязаны к антителу. А «защелка», крепящая семь противоопухолевых «бомб» к антителу – это реакция алкин-азидного присоединения, изобретенная Фокиным.
Выражаясь метафорически, если химиотерапия – это ковровая бомбардировка, наносящая вред всему организму – и только чуть больший самой опухоли, то созданный при помощи метода CuACC препарат – это высокоточное оружие. Выручка от продажи препарата сейчас уже превышает миллиард долларов в год.
Еще одно применение метода, используемое ежедневно – это секвенирование (установление порядков нуклеотидов) ДНК или РНК. Один из новых методов секвенирования использует клик-реакцию для «прочтения» генетического кода.
ClickSeq – это метод секвенирования РНК, который использует биоконъюгацию в качестве альтернативы фрагментации на этапе подготовки библиотеки, что позволяет снизить частоту ошибок по сравнению со стандартными методами секвенирования. Метод коммерциализован и используется в стандартных секвенаторах.
Литература:
Л. Стрельникова. Метод Фокина — Шарплесса. Идеальная химия и совсем не идеальная премия. «Химия и жизнь», 2022 № 10
Kolb H.C., Finn M.G., Sharpless K.B. Angew. Chem. Int. Ed. 2001, 40, 2004.
Huisgen, R. (1961). Centenary Lecture - 1,3-Dipolar Cycloadditions. Proceedings of the Chemical Society of London: 357. doi:10.1039/PS9610000357.
Christian W. Tornøe; Caspar Christensen & Morten Meldal (2002). Peptidotriazoles on Solid Phase: [1,2,3]-Triazoles by Regiospecific Copper(I)-Catalyzed 1,3-Dipolar Cycloadditions of Terminal Alkynes to Azides. Journal of Organic Chemistry. 67 (9): 3057–3064. doi:10.1021/jo011148j
https://hij.ru/read/29754/?ysclid=miwpyw5sag975638598
A. Salic, T. J. Mitchison PNAS 2008
Dieterich, D., Hodas, J., Gouzer, G. et al. In situ visualization and dynamics of newly synthesized proteins in rat hippocampal neurons. Nat Neurosci 13, 897–905 (2010). https://doi.org/10.1038/nn.2580
Syed, Y.Y. Sacituzumab Govitecan: First Approval. Drugs 80, 1019–1025 (2020). https://doi.org/10.1007/s40265-020-01337-5
https://www.illumina.com/science/sequencing-method-explorer/kits-and-arrays/clickseq.html
Routh A., Head S. R., Ordoukhanian P. and Johnson J. E. (2015) ClickSeq: Fragmentation-Free Next-Generation Sequencing via Click Ligation of Adaptors to Stochastically Terminated 3'-Azido cDNAs. J Mol Biol 427: 2610-2616
Chang M. W., Okulicz J. F., Johnson J. E. and Torbett B. E. (2015) CoVaMa: Co-Variation Mapper for disequilibrium analysis of mutant loci in viral populations using next-generation sequence data. Methods 91: 40-47
Основные публикации лауреата:
Rostovtsev, V. V.; Green, L. G.; Fokin, V. V.; Sharpless, K. B. A Stepwise Huisgen Cycloaddition Process: Copper(I)-Catalyzed Regioselective "Ligation" Of Azides and Terminal Alkynes Angew.Chem. Int. Ed. 2002, 41, 2596-2599.
Whiting, M.; Fokin, V. V. Copper-Catalyzed Reaction Cascade: Direct Conversion of Alkynes into N-Sulfonylazetidin-2-Imines Angew. Chem. Int. Ed. 2006, 45,3157-3161.
Cassidy, M. P.; Raushel, J.; Fokin, V. V. Practical Synthesis of Amides from in Situ Generated Copper(I) Acetylides and Sulfonyl Azides Angew. Chem. Int. Ed. 2006, 45, 3154-3157.
Worrell, B.T.; Malik, J.A.; Fokin, V.V. Direct Evidence of a Dinuclear Copper Intermediate in Cu(I)-Catalyzed Azide–Alkyne Cycloadditions. Science 2013, 340, 457-460.
Rillahan, C. D.; Macauley, M. S.; Schwartz, E.; He, Y.; McBride, R.; Arlian, B. M.; Rangarajan, J.; Fokin, V. V.; Paulson, J. C. Disubstituted sialic acid ligands targeting siglecs CD33 and CD22associated with myeloid leukaemias and B cell lymphomas Chem. Sci. 2014, 5, 2398.
Oakdale J.S.; Sit R.K., Fokin V.V. Ruthenium-Catalyzed Cycloadditions of 1-Haloalkynes with Nitrile Oxides and Organic Azides: Synthesis of 4-Haloisoxazoles and 5-Halotriazoles. Chem - Eur J.2014; 20, 11101.
Dong J., Sharpless K.B., Kwisnek L, Oakdale J.S., Fokin V.V. SuFEx-Based Synthesis of Polysulfates. Angew Chem, Int Ed. 2014; 53, 9466.
Arunrungvichian, K.; Boonyarat, C.; Fokin, V. V.; Taylor, P.; Vajragupta, O. Cognitive Improvements in a Mouse Model with Substituted 1,2,3-Triazole Agonists for Nicotinic AcetylcholineReceptors. ACS Chem. Neurosci. 2015, 6, 1331.
Oakdale, J. S.; Kwisnek, L.; Fokin, V. V. Selective and Orthogonal Post-Polymerization Modification using Sulfur(VI) Fluoride Exchange (SuFEx) and Copper-Catalyzed Azide-Alkyne Cycloaddition(CuAAC) Reactions. Macromolecules 2016, 49, 4473.
Eremin, D. B., Fokin, V. V., “On-Water Selectivity Switch in Microdroplets in the 1,2,3-Triazole Synthesis from Bromoethenesulfonyl Fluoride.” J. Am. Chem. Soc. 2021, 143, 18374-18379.
Aggarwal, S., Richards, W. J., Fokin, V. V., “Generation and Aerobic Oxidation of Azavinyl Captodative Radicals.” J. Am. Chem. Soc. 2023, 145 (45), 24452–24458.
Aggarwal, S., Vu, A., Eremin, D. B., Persaud, R., Fokin, V. V., “Arenes participate in 1,3-dipolar cycloaddition with in situ-generated diazoalkenes.” Nat. Chem. 2023, 15, 764-772.
Grotsch, K., Sadybekov, A. V., Hiller, S., Zaid, S., Eremin, D., Le, A., Liu, Y., Smith, E. C., Illiopoulis-Tsoutsouvas, C., Thomas, J., Aggarwal, S., Pickett, J. E., Reyes, C., Picazo, E., Roth, B. L.,Makryannis, A., Katritch, V., Fokin, V. V., “Virtual Screening of a Chemically Diverse “Superscaffold” Library Enables Ligand Discovery for a key GPCR Target.” ACS Chem. Biol. 2024 19 (4), 866–874.
Majumder, T., Eremin, D.B., Delibas, B., Sarkar, A., Fokin, V., and Dawlaty, J.M. Calibrating the Oxidative Capacity of Microdroplets. Angew. Chem. Int. Ed. 2025, 64, e202414746
Ключевые 9 из 31 патента лауреата:
1. Fokin V. V., Sharpless K. B., Green L. G., Rostovtsev V. V., Himo F. Copper-Catalyzed Ligation of Azides and Acetylenes. U. S. Patent 7,375,234 (2008)
2. Fokin V. V., Sharpless K. B., Green L. G., Rostovtsev V. V., Himo F. Copper-Catalyzed Ligation of Azides and Acetylenes. U. S. Patent 7,763,736 (2010)
3. Fokin, V.V., Jia, G., Sharpless, K.B. Ruthenium-Catalyzed Cycloaddition of Alkynes and Organic Azides, U.S. Patent 8,372,986 (2012).
4. Fokin, V., Finn, M.G.; Sharpless, K.B. Polymeric Materials via Click Chemistry, U.S. Patent 8,101,238 (2012).
5. Gastaminza, P., Chisari, F.V., Pitram, S.M., Fokin, V.V.,Sharpless, K.B., Krasnova, L.B., Dong, J.: Preparation and Compositions of Piperazine Compounds as Inhibitors of Hepatitis C Virus Infection. Patent WO2010014744A1 (2010).
6. Hein J.E., Tripp J.C., Krasnova L., Sharpless K.B., Fokin V.V.; Copper Catalyzed Cycloaddition of Organic Azides and 1-Haloalkynes to Prepare 1,2,3-Triazoles. Patent WO2011019799A2 (2011).
7. Taylor, P., J. Yamauchi, T. T. Talley, K. Arunrungvichian, O. Vajragupta and V. Fokin (2016). Preparation of Substituted 1,2,3-Triazoles as Selective Α7 Nicotinic Receptoragonists WO2016154434A1
8. Taylor, P., Radic, Z., Fokin, V. Catalytic Scavengers of Organophosphates to Potentiate Butyrylcholinesterase (Hbche) as a Catalytic Bioscavenger and Methods Formaking and Using Them. US 10,172,831 (2018)
9. Taylor, P., Camacho-Hernandez, G., Sharpless, K., Finn, M. G., Fokin, V. Selective alpha-7 Nicotinic Receptor Agonists and Methods for Making Andusing them US 10,308,638 (2019) 10. Katritch, V., Fokin, V. V., Zaidi, S., Thomas, J. Preparation of Opioid Receptor Antagonoists. WO2021178405 (2021).
